Frovatriptan
| Strukturformel | ||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
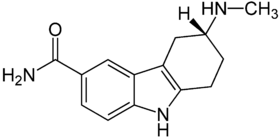
| ||||||||||||||||
| Allgemeines | ||||||||||||||||
| Freiname | Frovatriptan | |||||||||||||||
| Andere Namen |
(R)-6-(Methylamino)-5,6,7,8-tetrahydrocarbazol-3-carbamid | |||||||||||||||
| Summenformel | C14H17N3O | |||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||
| ||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||
| ATC-Code | ||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||
| Wirkmechanismus |
Selektiver 5-HT1-Rezeptor Agonist | |||||||||||||||
| Eigenschaften | ||||||||||||||||
| Molare Masse | 243,30 g·mol−1 | |||||||||||||||
| Sicherheitshinweise | ||||||||||||||||
| ||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||
Frovatriptan ist ein Serotonin-Rezeptor-Agonist aus der Gruppe der Triptane, der als Arzneistoff zur Akuttherapie der Migräne zugelassen ist. Darüber hinaus zeigt er Wirksamkeit in der vorbeugenden Behandlung des Cluster-Kopfschmerzes.[2][3] Frovatriptan wurde von Vernalis entwickelt und wird in Deutschland von Berlin-Chemie und Kohlpharma angeboten. Es unterliegt der ärztlichen Verschreibungspflicht.
Chemie
[Bearbeiten | Quelltext bearbeiten]Frovatriptan gehört der Gruppe der Triptane an. Es ist ein ringgeschlossenes Derivat des 5-HT1/7-Rezeptoragonisten 5-Carboxamidotryptamin und ähnelt strukturell dem Serotonin.
Pharmakologie
[Bearbeiten | Quelltext bearbeiten]Wirkmechanismus
[Bearbeiten | Quelltext bearbeiten]Frovatriptan ist ein hochpotenter Agonist an den Serotonin-Rezeptoren 5-HT1B und 5-HT1D, welche auf zerebralen Blutgefäßen und präsynaptisch auf Neuronen vorkommen. Eine Aktivierung dieser Rezeptoren durch Frovatriptan führt somit während eines Migräneanfalls einerseits zu einer Konstriktion der dilatierten zerebralen Blutgefäße und andererseits zu einer Verminderung der Ausschüttung von Entzündungsmediatoren.[4] Eine Aktivierung von 5-HT1B-Rezeptoren wird jedoch auch mit kardiovaskulären Nebenwirkungen in Verbindung gebracht.
Mit einer Halbwertzeit von 26 h besitzt Frovatriptan innerhalb der Gruppe der Triptane die mit Abstand längste Wirkdauer. Daher konnte unter der Therapie mit Frovatriptan die Wiederholungsrate der Migräneattacken stärker gesenkt werden als mit anderen Triptanen.
Zusätzlich aktiviert Frovatriptan in hohen Dosen auch 5-HT7-Rezeptoren.[5] Auf Grund dieses zusätzlichen Wirkmechanismus wurde vor der Markteinführung ein günstigeres Nutzen-Risiko-Verhältnis erwartet, was sich jedoch nicht bestätigte.
Nebenwirkungen
[Bearbeiten | Quelltext bearbeiten]Häufiger (bei 1 von 100 Personen) können Übelkeit, Mundtrockenheit, Verdauungsstörungen und Bauchschmerzen beobachtet werden. Ebenfalls häufig sind Kopfschmerzen, Schwindelgefühl und Parästhesien in den Armen und Beinen sowie verändertes Berührungsempfinden und extreme Schläfrigkeit. Auch Hitzewallungen, gegebenenfalls mit Hautrötungen sowie vermehrtes Schwitzen werden oft beobachtet.
Gelegentlich (bei 1 von 1000 Personen) kommt es zu Geschmacksstörungen, Tremores, Konzentrationsschwäche, Lethargie, gesteigertem Berührungsempfinden und unwillkürlichen Muskelkontraktionen. Auch Magenbeschwerden wie Durchfall oder Blähungen im Magen und/oder Darm können beobachtet werden.
An dieser Stelle muss erwähnt werden, dass viele dieser Nebenwirkungen häufig nicht klar auf den Wirkstoff zurückgeführt werden können, da auch die Migräne selbst ähnliche oder deckungsgleiche Symptome umfasst.
Eine der charakteristischen, aber seltenen Nebenwirkungen der Anwendung von Frovatriptan sind der Angina Pectoris ähnliche Druck- und Beklemmungsgefühle der Brust, die auf eine Konstriktion der Herzkranzgefäße zurückgeführt werden. Ein Blutdruckanstieg ist ebenfalls bei einigen Patienten zu beobachten.
Wechselwirkungen
[Bearbeiten | Quelltext bearbeiten]Frovatriptan sollte nicht mit Ergotamin kombiniert eingesetzt werden, da eine erhöhte Gefahr von Koronarspasmen besteht. Die gleichzeitige Einnahme mit Serotonin-Wiederaufnahmehemmern (SSRI), wie z. B. Fluoxetin, Paroxetin, Sertralin und Citalopram, selektiven Serotonin- und Noradrenalin-Wiederaufnahmehemmern (SNRI) oder dem pflanzlichen Antidepressivum Johanniskraut kann die Wirkungen und Nebenwirkungen von Frovatriptan verstärken. Die amerikanische Gesundheitsbehörde FDA warnt in diesem Zusammenhang vor der potenziell lebensbedrohlichen Wechselwirkung des Serotonin-Syndroms (=der Körper kumuliert zu viel Serotonin im Nervensystem).[6] Symptome des Serotoninsyndroms können Ruhelosigkeit, Halluzinationen, Verlust der Koordination, schnellen Herzschlag, Blutdruckschwankungen, erhöhte Körpertemperatur, gesteigerte Reflexe, Übelkeit, Erbrechen und Durchfall einschließen. Absolute Vorsicht ist auch bei gemeinsamer Anwendung von Frovatriptan mit MAO-Hemmern geboten.
Handelsnamen
[Bearbeiten | Quelltext bearbeiten]Allegro (D), Eumitan (A), Frovamig (A), Frovalan (A), Menamig (CH)
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Datenblatt FROVATRIPTAN RACEMATE bei Sigma-Aldrich, abgerufen am 26. Dezember 2022 (PDF).
- ↑ Siow HC, Pozo-Rosich P, Silberstein SD.: Frovatriptan for the treatment of cluster headaches. Cephalalgia. 2004; 24(12): 1045–1048; PMID 15566418; doi:10.1111/j.1468-2982.2004.00734.x.
- ↑ S1-Leitlinie Clusterkopfschmerz und trigeminoautonome Kopfschmerzen der Deutschen Gesellschaft für Neurologie (DGN). In: AWMF online (Stand 2015).
- ↑ Limmroth V: Wirkungsmechanismus der Triptane. In: Pharmazie in unserer Zeit. 31. Jahrgang, Nr. 5, 2002, S. 458–61, doi:10.1002/1615-1003(200209)31:5<458::AID-PAUZ458>3.0.CO;2-G, PMID 12369163.
- ↑ Jähnichen S, Glusa E, Pertz HH: Evidence for 5-HT2B and 5-HT7 receptor-mediated relaxation in pulmonary arteries of weaned pigs. In: Naunyn Schmiedebergs Arch Pharmacol. 371. Jahrgang, Nr. 1, Januar 2005, S. 89–98, doi:10.1007/s00210-004-1006-6, PMID 15726452 (englisch).
- ↑ FDA Public Health Advisory: Combined Use of 5-Hydroxytryptamine Receptor Agonists (Triptans), Selective Serotonin Reuptake Inhibitors (SSRIs) or Selective Serotonin/Norepinephrine Reuptake Inhibitors (SNRIs) May Result in Life-threatening Serotonin Syndrome, vom 19. Juli 2006 (englisch).